LU • Ordnungszahl 71

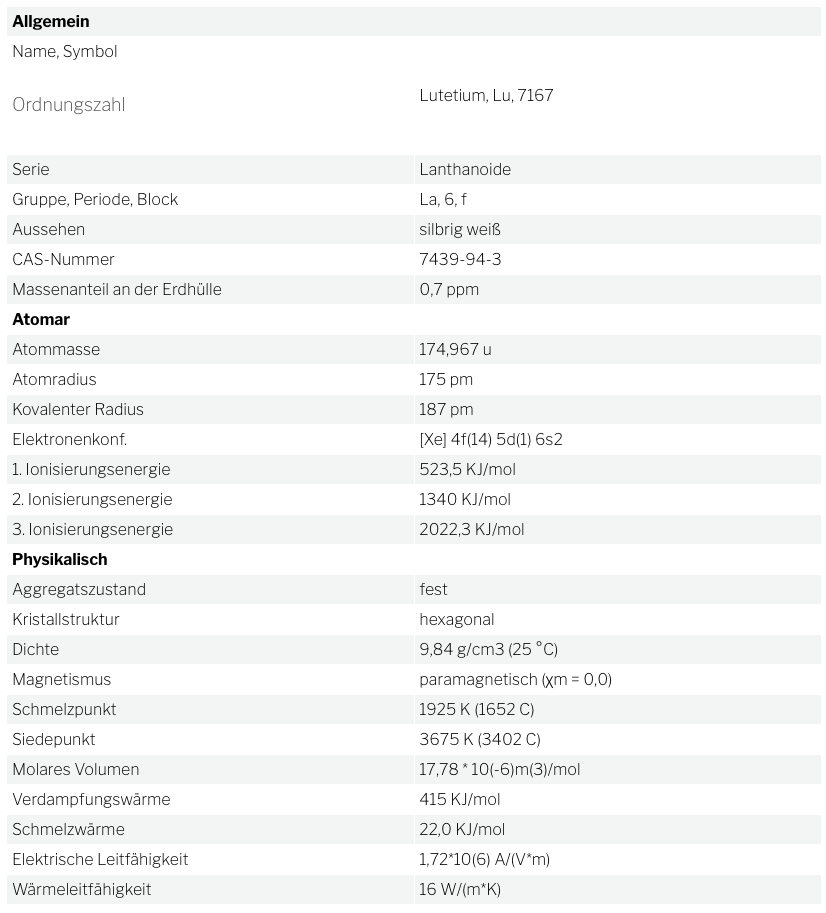
Lutetium
Lutetium ist ein silberglänzendes Metall und ist das letzte und schwerste Element der Lanthanoidenreihe. Lutetium zählt zu den schweren seltenen Erden.
Es ist das seltenste Element, das unter den Seltenen Erden am schwierigsten zu gewinnen ist. Reines Lutetiumoxid oder -metall ist eines der kostbarsten Seltenerd-Materialien.
Die wichtigste Eigenschaft von Lutetium ist seine extrem hohe Härte und Dichte für ein Metall der Seltenen Erden.
Seine Hauptanwendung liegt in der Nuklearmedizin.
Lutetium wurde 1905 von drei Wissenschaftlern unabhängig voneinander entdeckt: Carl Auer von Welsbach, Charles James und Georges Urbain, der es nach dem römischen Namen von Paris, Lutetia, benannte. Im deutschen Sprachraum wurde es bis 1949 meist als Cassiopeium (chemisches Zeichen Cp) bezeichnet.
Xenotim ist das wichtigste Mineral für Lutetium. Es reichert bevorzugt die schweren Seltenen Erden (einschließlich Yttrium) an. Lutetium ist hier oft in höheren Konzentrationen enthalten als in anderen Mineralien.
Wichtigstes Herstellungsland ist China.
Nach einer aufwändigen Abtrennung der anderen Lutetiumbegleiter wird das Oxid mit Fluorwasserstoff zum Lutetiumfluorid umgesetzt. Anschließend wird dieses mit Calcium unter Bildung von Calciumfluorid zum metallischen Lutetium reduziert. Abtrennung verbleibender Calciumreste und Verunreinigungen erfolgen in einer zusätzlichen Umschmelzung im Vakuum.
Die wichtigste und bedeutendste Verwendung von Lutetium liegt in der modernen Medizin, in der Krebstherapie.
Lutetium-177 (¹⁷⁷Lu) ist ein radioaktives Isotop, das als theranostisches Agens eingesetzt wird. Dieser Begriff kombiniert "Therapie" und "Diagnostik" und beschreibt einen revolutionären Ansatz in der Onkologie.
Für die Diagnose sendet Lutetium eine geringe Menge Gammastrahlung aus und macht den Tumor für Ärzte über eine SPECT-Kamera (Single-Photon Emission Computed Tomography) sichtbar.
Bei der Therapie sendet ¹⁷⁷Lu Beta-Strahlung (β⁻-Teilchen) aus. Diese Teilchen haben eine genau passende Energie, um Krebszellen gezielt zu zerstören, während das umliegende gesunde Gewebe weitgehend verschont bleibt.
Spezielle Einsatzgebiete für Lutetium sind Szintillatoren (in Detektoren) für die Krebsdiagnostik. Lutetiumorthosilikat (LSO) und Lutetiumyttriumorthosilikat (LYSO) sind extrem effiziente Kristalle, die in medizinischen PET-Scannern (Positronen-Emissions-Tomographie) verwendet werden.
Lutetiumverbindungen werden zudem als hochaktive Katalysatoren in der petrochemischen Industrie eingesetzt, beispielsweise bei der Polymerisation und beim Cracken von Erdöl verwendet.
Das silbergraue Metall ist sehr weich, gut dehnbar und schmiedbar. In trockener Luft ist Lutetium recht beständig, in feuchter Luft läuft es grau an. Bei höheren Temperaturen verbrennt es zum Sesquioxid Lu2O3. Mit Wasser reagiert es sehr langsam unter Wasserstoffentwicklung zum Hydroxid. In Mineralsäuren löst es sich unter Bildung von Wasserstoff auf.
In seinen Verbindungen liegt es in der Oxidationsstufe +3 vor, die Lu3+-Kationen bilden in Wasser farblose Lösungen.